材料制备与检测
实验讲义
南阳理工学院生物与化学工程学院
化工工艺教研室
实验1 Pb2+吸附剂的制备及吸附条件研究
一、目的要求
以资源整合再利用,从可持续发展的角度出发,研究Pb2+吸附剂的制备及吸附条件。
二、原理
利用水果皮——天然吸附材料,吸附重金属离子。
三、主要试剂及仪器
乙二胺四乙酸二钠、无砷金属锌、盐酸、氨水、氯化铵、乙酸铅、冰乙酸、二甲酚橙、酸无水乙酸钠 |
四、实验方法
1、化学活化法制备吸附剂
先用水洗净香蕉皮,再用蒸馏水冲洗并晾干,加入一定量的化学试剂浸渍活化一定时间,然后用蒸馏水冲洗并晾干,在一定的温度下锻烧一定时间,最后用粉碎机粉碎到40-100的吸附剂粉粒。
2、铅离子的吸附实验
取50mL一定浓度的含Pb2+溶液,置于250mL的三口烧瓶中,通过滴加氨水或乙酸调节pH为一定值后加入某一锻烧温度锻烧一定时间后的一定质量酸处理香蕉皮吸附剂,于一定温度条件中转速下搅拌反应一定时间,过滤,取滤液测定残留Pb2+浓度。
3、铅离子浓度的测定方法
采用EDTA二钠盐滴定法,用二甲酚橙作为显色剂, CH3COONa-CH3COOH为缓冲液PH=5.5-6 ;滴定终点的判断:废液颜色由酒红色变成亮黄色。
4、吸附量及去除率的计算
本实验吸附量和去除率计算根据式(2—1)和式(2—2)。
q=(Co—Ct)VM/m (2—1)
Y(%)=(Co—Ct)/Co (2—2)
式中:
q—吸附量(g/g);
Co—溶液起始浓度(mol/L);
Ct—溶液在t时刻的浓度(mol/L);
V—溶液体积(L);
M—溶液中重金属的摩尔质量(g/moL);
m—吸附剂用量(g);
Y—去除率(%);
六、思考题
1、为什么可以利用香蕉皮吸附Pb2+?
2、怎么进行等温吸附方程的拟合?
参考资料
[1]陈坚.污泥活性炭的制备及其对铅镉的吸附研究[D]:中山大学,2009:1-15
[2]马静.天然植物材料作为吸附剂处理低浓度重金属废水的研究[D].湖南大学.2007:2-8.
实验2 丙烯酸系水凝胶的制备
一、目的要求
掌握功能高分子材料水凝胶的制备方法及吸水性能的测定。
二、实验原理
丙烯酸在常温下与氢氧化钠发生中和反应, 然后与丙烯酰胺一起在引发剂、交联剂存在下, 于一定温度下发生聚合交联反应。,
三、主要试剂及仪器
丙烯酸(AA)、丙烯酰胺(AM)、氢氧化钠、N,N’-亚甲基双丙烯酰胺(MBA)、过硫酸铵、
电动搅拌器、烧杯、水浴锅、量筒
四、实验步骤
在烧杯中加入一定量的丙烯酸,用一定量氢氧化钠中和;在室温下加入适量的丙烯酰胺、交联剂并搅拌均匀,加入过硫酸铵引发剂,将烧杯置于70℃的水浴锅中,8min快速聚合制得吸水树脂;将树脂置于80℃烘箱中烘至恒重,干燥后的产品破碎,得到白色或浅黄色样品,密封包装。
五、注意事项:
1.丙烯酸预中和时容易出现沉淀,加入少量蒸馏水溶解可解决。
2.引发剂需配制成溶液后加入。
3.烘干温度高时树脂产品容易发黄。
六、产品性能分析:
先准确称量所取产品质量,常为1克左右,放入1000毫升烧杯中,然后加入大量蒸馏水,使其充分膨胀,经吸水完毕后(通常是目测,当看到膨胀后树脂内没有气泡时,便认为吸水完毕)用滤布滤去未吸蒸馏水,用托盘天平称量吸水后树脂质量,根据下式计算吸水倍率.
树脂吸水率=干吸水剂产品吸水量/干吸水剂质量
实验3 环氧树脂的制备
环氧树脂是指含有环氧基的聚合物,它有多种类型,如:环氧氯丙烷与酚醛缩合物反应
生成的酚醛环氧树脂、与甘油反应生成的甘油环氧树脂、与二酚基丙烷(双酚A)反应生成的二丙烷环氧树脂等。环氧氯丙烷是主要单体,它可以与各种多元酚类、多元醇类反应,生成各类环氧树脂。在环氧树脂结构中有羟基、醚基和极为活泼的环氧基存在,使环氧分子与相邻界面产生了较强的分子间作用力,而且环氧基团则与介质表面,特别是金属表面上的游离键起反应,形成化学键。因而环氧树脂具有很高的粘合力,用途很广,商业上称作“万能胶”。此外,环氧树脂还可以作涂料、层压材料、浇铸、浸渍及模具等用途。
一、目的要求
本实验将通过环氧氯丙烷与双酚A缩聚制取双酚A型环氧树脂。熟悉该类环氧树脂的
实验室制法,掌握环氧值的测定方法并了解环氧树脂的实用方法和性能。
二、原理
双酚A型环氧树脂产量最大,用途最广,有通用环氧树脂之称。它是环氧氯丙烷与二酚基丙烷在氢氧化钠作用下聚合而得。
其反应式为:
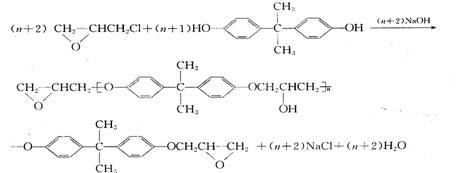
根据不同的原料配比,不同操作条件(如反应介质、温度和加料顺序),可制得不同的分子量的环氧树脂。现生产上将双酚A型环氧树脂分为高分子量、中分子量及低分子量三种。分子量对软化点的影响如图2-1。通常把软化点低于50 ℃(平均聚合度元n< 2)的称为低分子量树脂或称软树脂;软化点在50~90℃之间(n在2~5之间)称为中等分子量树脂;软化点;在100℃以上(n>5)称为高分子量树脂。环氧树脂的分子量与单体的配料比有密切关系,当反应条件相同,环氧氯丙烷与双酚A的物质的量越接近于1时,产物的软化点越高,分子量越大。
由于环氧树脂在未固化前呈热塑性的线性结构,使用时必须加入固化剂。固化剂与环氧
树脂的环氧基等反应,变成网状的热固性大分子成品。固化剂的种类很多,最常用的有多元
胺、酸酐及羧酸等。其交联过程可表示为(以二元胺为交联剂):
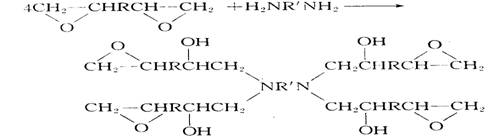
上述分子两端的环氧基还可继续固化,交联成网状结构大分子。
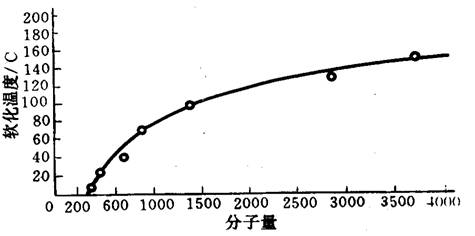
图1-1环氧树脂的分子量对软化点的影响
三、仪器和试剂
三口瓶、冷凝管、滴液漏斗、分液漏斗、蒸馏瓶。
双酚A、环氧氯丙烷、甲苯、20%NaOH溶液、25%盐酸溶液。
四、实验步骤
1.树脂制备:
将22.5g双酚A(0.lmol)、28g环氧氯丙烷(0.3mol)加入到250ml三口瓶中。搅拌下缓慢升温至约55℃,待双酚A全部溶解后,开始滴加20%NaOH溶液40ml至三口瓶中,保持反应温度在70℃以下,若反应温度过高,可减慢消加速度,约0·5 h滴加完毕。在90 ℃左右继续反应2h,在搅拌下用25%酸中和反应液至中性(注意充分搅拌,使中和完全)。向瓶内加去离子水30ml,甲苯60ml。充分搅拌并倒入250m1分液漏斗中,静置片刻,分去水层,再用去离子水洗涤数次至水相中无 CI―离子( AgNO3溶液检验),分出有机层,减压蒸去甲苯及残余的水。蒸馏瓶留下浅黄色粘稠液体即为环氧树脂。
五、结果与讨论
线型环氧树脂外观为黄色至青铜色的粘稠液体或脆性固体,易溶于有机溶剂中。未加固化剂的环氧树脂有热塑性,可长期储存而不变质。其主要参数是环氧值,固化剂的用量与环氧值成正比,固化剂的用量对成品的机械性能影响很大,必须控制适当。
六、性能测试
1. 环氧值的测定
环氧值是指每100g环氧树脂中含环氧基的当量数。它是环氧树脂质量的重要指标,是计算固化剂用量的依据。树脂的分子量越高,环氧值相应降低,一般低分子量环所树脂的环氧值在0.48-0.57之间。另外,还可用环氧基百分含量(每100g树脂中含有的环氧基克数)和环氧当量(一个环氧基的环氧树脂克数)来表示,三者之间的互换关系如下:
环氧值=环氧基百分含量/环氧基分子量=1/环氧当量
因为环氧树脂中的环氧基在盐酸的有机溶液中能被HCl开环,所以测定所消耗的HCl的量,即可算出环氧值。其反应式为:
 n CH2 —CH2 + HCl ~CH—CH~
n CH2 —CH2 + HCl ~CH—CH~




 O OH Cl
O OH Cl
过量的HCl用标准NaOH-乙醇液回滴。
对于分子量小于1500的环氧树脂,其环氧值的测定用盐酸-丙酮法测定,分子量高的用盐酸-砒啶法,具体操作如下:
准确称取1g左右环氧树脂,放入150 ml的磨口锥形瓶中,用移液管加入25 ml盐酸-丙酮溶液,加塞摇动至树脂完全溶解,放置1h。加入酚酞指示剂3滴,用NaOH--乙醇溶液滴定至浅粉红色,同时按上述条件做空白实验2次。
环氧值EPV=(V0-V1)N/10W
式中V0,V1------表空白和样品滴定所消耗的NaOH的量;
N--------溶液的当量浓度;
W-------树脂重量。
注: 盐酸-丙酮溶液: 2 ml浓盐酸溶于80 ml丙酮中,混合均匀。
NaOH—乙醇标准溶液: 将4gNaOH溶于是100 ml乙醇中,用标准邻苯二甲酸氢钾溶液标定,酚酞作指示剂。
2.性能测定:
(1)分别准备两小块木片和铝片,木片用砂纸打磨擦净,铝片用酸性处理液(10份
K2Cr2O7, 50份浓 H2SO4,340份 H2O配成)处理10--15min, 取出用水冲洗后晾干。
(2)用干净的表面皿称取4g环氧树脂,加入0.3g乙二胺用玻璃棒调匀,分别取少量均匀涂于木片或铝片的端面约1cm的范围内,对准胶合面合拢,压紧,放置待固化后观察粘结效果。或在教师指导下通过剪切实验,可定量的测定粘结效果。
七、思考题
1.在合成环氧树脂的反应中,若NaOH的用量不足,将对产物有什么影响?
2.环氧树脂的分子结构有何特点?为什么环氧树脂具有良好的粘结性能?
3.为什么环氧树脂使用时必须加人固化剂?固化剂的种类有哪些?
参考资料
[1]上海树脂厂编.环氧树脂生产与应用.石油化学工业出版社,1974
[2]欧阳国恩,欧国荣主编.复合材料试验技术.武汉工业大学出版社,1993
[3]胡学贵编著.高分子化学及工艺学.化学工业出版社,1991
实验4 玻璃钢(FRP)平板制品手糊成型
一、目的要求
了解掌握玻璃钢手糊成型的基本方法,熟悉玻璃钢手糊制品的制备原理。
二、原理
FRP手糊成型工艺是FRP制品生产中使用最早的一种成型工艺。尽管随着FRP工业
的迅速发展,新的成型技术不断涌现,但在整个 FRP工业发展过程中,手糊成型工艺仍占有重要地位。手糊成型工艺操作简便,设备简单,投资少,不受制品形状尺寸限制,可以根据设计要求,铺设不同厚度的增强材料。手糊成型特别适合于制作形状复杂、尺寸较大、用途特殊的FRP制品。但手糊成型工艺制品质量不够稳定,不易控制,生产效率低,劳动条件差。
手糊成型工艺过程可概括如下:
树脂胶液配制
增强材料准备:I——增强材料浸渍
模具准备-----一涂脱模剂——手糊——固化脱模修整——质量检验
三、设备和原料
剪刀 1把
钢皮尺 1只
台秤 1台
玻璃板(钢化)2块 (40cm ×40cm ×0.5cm)
涤纶薄膜 2块(50cm×50cm)
玻璃烧杯 1只
玻璃棒 1只
刮刀 1只
0.4 mm厚的无碱无捻玻璃纤维方格布 若干
环氧树脂:(实验室合成)
乙二胺 。
四、实验步骤
1.裁剪0.4mm厚玻璃布 150×150mm 8块,并称重。
2.按FRP手糊制品50%的含胶量称取环氧树脂。按每100份(wt)树脂加入13份乙二胺,充分搅拌均匀,再加入2—4份丙酮溶液,充分搅拌均匀待用。
3.在玻璃板上铺放好涤纶薄膜,在中央区域倒上少量树脂,铺上一层玻璃布、用刮刀刮涂,使树脂充分浸透玻璃布后,再铺上第二层,再用刮刀刮涂,如此重复直至铺完所有的玻璃布。最后在面上盖上另一张涤纶薄膜,用干净的刮刀在薄膜上推赶气泡。要求既要保留树脂又要赶尽气泡。气泡赶尽后,在平整的表面上再压上另一块玻璃板。
4.室温下固化24h后,检查制品的固化情况。
五、实验讨论
实验时应注意,涂刷用力要沿布的径向,顺着一个方向从中间向两边把气泡赶尽使玻璃布贴合紧密,含胶量均匀。铺第一、第二层布时,树脂含量应高些,这样有利于浸透织物并排出气泡。
六、思考题
分析本实验手糊制品产生缺陷的原因及解决办法。
参考资料
[1] 欧国荣等编.复合材料工艺与设备.华东化工学院出版社,1991.5
[2] 施美英编.复合材料专业实验,1995.9

