高分子化学实验讲义
南阳理工学院生物与化学工程系 应用化学教研室
张群安 史政海
二0一五年十二月
实验1 聚乙烯醇缩甲醛的制备
早在1931年,人们就已经研制出聚乙烯醇(PVA)的纤维,但由于 PVA的水溶性而无法实际应用。利用“缩醛化”减少其水溶性,就使得PVA有了较大的实际应用价值。用甲醛进行缩醛化反应得到聚乙烯醇缩甲醛(PVF)。PVF随缩醛化程度不同,性质和用途有所不同。控制缩醛在35%左右,就得到了人们称为“维纶’的纤维(vinylon)。维纶的强度是棉花的1.5~2.0倍,吸湿性5%,接近天然纤维,又称为“合成棉花”。
在PVF分子中,如果控制其缩醛度在较低水平,由于PVF分子中含有羟基、乙酸基和醛基,因此有较强的粘接性能,可作胶水使用,用来粘结金属、木材、皮革、玻璃、陶瓷、橡胶等。
一、目的要求:
本实验将通过PVA的缩醛化制备胶水,了解乙烯醇缩醛化的反应原理,并了解高聚物的官能团侧基反应的知识。
二、原理:
聚乙烯醇缩甲醛是利用聚乙烯醇与甲醛在盐酸催化的作用下而制得的。其反应式如下
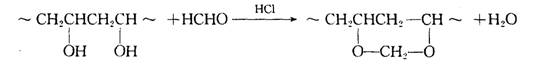
高分子链上的羟基未必能全部进行缩醛化反应,会有一部分羟基残留下来,本实验是合成水溶性聚乙烯醇缩甲醛胶水,反应过程中需控制较低的缩醛度,使产物保持水溶性。如若反应过于猛烈,则会造成局部高缩醛度,导致不溶性物质存在于胶水中,影响胶水质量。因此在反应过程中,要特别注意严格控制催化剂用量、反应温度、反应时间及反应物比例等因素。
三、仪器和试剂:
仪器:三口瓶、搅拌器、温度计、球形冷凝管、量筒、培养皿;
试剂:PVA、甲醛水溶液(40%工业甲醛)、盐酸、NaOH、PH试纸。
四、实验步骤:
在250ml三口瓶中,加入 160ml去离子水、17gPVA、在搅拌下升温至80~90℃使其溶解(注意:先加入水,而后加入PVA,采用慢加快搅的方法使PVA溶解,避免快加时容易出现PVA成团难以溶解的现象)。等PVA全部溶解后(呈透明状溶液),于90℃左右加人3ml甲醛搅拌,滴加 1:4盐酸(体积比:1体积盐酸+4体积水)溶液,控制反应体系PH值为1~3,保持反应温度90℃左右。继续搅拌,反应体系逐渐变稠。当体系中出现气泡或有絮状物(交联)产生时,立即迅速加入 1.5 ml 8%的 NaOH溶液,调节PH值为 8~9,冷却出料,所获得无色透明粘稠液体,即得市售胶水。
五、结果与讨论:
由于缩醛化反应的程度较低,胶水中尚含有未反应的甲醛,产物往往有甲醛的刺激性气味。缩醛基团在碱性环境下较稳定,故要调整胶水的PH值。
六、性能测试:测试制品的粘度、PH值、粘结力。
粘度:用涂—4粘度计测定粘度并与标准样品比较。
PH值:用PH试纸测定胶水的PH值。
粘结力:用实验制得的胶水粘结纸张与标准样品比较。
七、思考题
1.产物为什么要把最终PH值调至8~9,试讨论缩醛化PVA对酸和碱的稳定性。
2.为什么缩醛度增加,水溶性会下降?
实验2 本体聚合MMA制有机玻璃板及其透光率测定
聚甲基丙烯酸甲酯(PMMA)具有优良的光学性能、密度小、机械性能、耐候性好。在航空、光学仪器工业、电器工业、日用品等方面有广泛用途。
本体聚合除了适合于实验室研究,还适用于制造板材和型材,所用设备也较简单。如单体聚合能力的初步测定、聚合动力学研究和竞聚率测定等。其优点是产品纯净,尤其可以制得透明制品,其缺点是散热困难,易发生凝胶效应,工业上常采取分段聚合的方式。
一、目的要求
本实验通过本体聚合MMA,掌握和了解有机玻璃的制造和操作技术,了解本体聚合技术的特点。
二、原理
MMA是含不饱和双键、结构不对称的分子,易发生聚合反应,其聚合热为56.5kJ/mol。 MMA在本体聚合中的突出特点是有“凝胶效应”,即在聚合过程中,当转化率达到10%~20%时,聚合速率突然加快,物料的粘度骤然上升,以致发生局部过热现象。其原因是由于随着聚合反应的进行,物料的粘度增大,活性增长链移动困难,致使其相互碰撞而产生的链终止下降;相反,单体分子扩散作用不受影响,因此活性链与单体分子结合进行链增长的速率不变,总的结果是聚合总速率增加,以致发生爆发性聚合。
由于本体聚会没有稀释剂存在,聚会热的排散比较困难,“凝胶效应”放出大量反应热,使产品含有气泡影响其光学性能。因此在生产中要通过严格控制聚合温度来控制聚合反应速率,以保证有机玻璃产品的质量。
预聚合有几个好处,一是缩短聚合反应的诱导期并使“凝胶效应”提前到来,以便在灌模前移出较多的聚合热,以利于保证产品质量;二是可以减少聚合时的体积收缩,因MMA由单体变成聚合体体积要缩小20%~22%,通过预聚合可使收缩率小于12%,另外浆液粘度大,可减少灌模的渗透损失。
三、仪器和试剂
玻璃片、透明胶带、脱膜剂硅油、烧杯、三口烧瓶、搅拌器、球形冷凝管.
MMA、过氧化二苯甲酰(BPO)。
四、实验步骤
一般分为下列几个主要步骤:(1)制模;(2)预聚合(制浆);(3)灌浆;(4)聚合;(5)脱模。
1.制模
取三块 40mm × 70mm硅玻璃片洗净并干燥。把三块玻璃片重叠,并将中间一块纵向抽出约30 mm,其余三断面用涤纶绝缘胶带封牢。将中间玻璃抽出,作灌浆用。
2.预聚合
在 100ml三角烧杯中加入 60g MMA,再称量 0.09g BPO,轻轻摇动至溶解,倒入三口烧瓶中。搅拌下于 85~90 ℃水浴中加热预聚合。观察反应的粘度变化至形成粘性薄浆(似甘油状或稍粘些),反应约需0.5~l h,迅速冷却至室温,将预聚合好的粘浆倒人烧杯,再真空脱气半小时(实验室暂时不做)。
3.灌浆
将脱气后的粘液慢慢灌入模具中,垂直放置10min赶出气泡,然后将模口包装密封。
4.聚合
将灌浆后的模具在40~50℃的烘箱内进行低温聚合10~12 h,当模具内聚合物基本成为固体时升温到95~100℃,保持1.5~2 h。
5.脱模
将模具缓慢冷却到 50~60 ℃,撬开硅玻璃片,得到有机玻璃板。
五、结果与讨论
本实验的关键在于预聚合,因为“凝胶效应”会产生大量的热,如果排除不及时,会发生爆聚,产生大量气泡,导致瓶内溶液成难溶的固体凝胶团,难以从瓶中取出,反应失败。如果预聚合反应进行得不够,则在灌浆后体积收缩严重,也会出现气泡或空洞,影响产品质量,甚至会由于单体挥发而无产品。为了产品脱模方便,可在硅玻璃片表面涂一层硅油,但量一定要少,否则影响产品的透光度。
六、思考题
1.MMA的本体聚合有何特点?制造有机玻璃的步骤有哪些?
2.本体聚合工艺中的关键是什么?采用什么措施来解决这些问题?
参考资料
珊瑚化工厂.有机玻璃.上海人民出版社,1974
实验3 丙烯酸酯树脂合成
一、实验目的
1.了解自由基型加聚反应的原理。
2.掌握丙烯酸酯溶液共聚合的合成原理和方法。
二、实验原理
聚丙烯酸酯溶液为无色或浅黄色透明粘稠液体,具有优良的粘接能力,可在较广的温度范围内使用。具有良好的成膜性,且耐老化性、腐蚀性良好,应用于汽车面漆。
丙烯酸酯单体的聚合反应是自由基型加聚反应属连锁聚合反应,整个过程包括链引发、链增长和链终止三个基元反应。链引发就是不断产生单体自由基的过程。常用的引发剂如过氧化合物和偶氮化合物,它们在一定温度下能分解生成初级自由基,它与单体加成产生单体自由基。生成的极为活泼的单体自由基不断迅速地与单体分子加成,生成大分子自由基。两个大分子自由基相遇,活泼的单电子相结合而使链终止。
加入适量的甲酯使漆膜有适中的硬度、强度,加入较多量的丁酯使漆膜有适中的柔韧性、抗冲击性能,加入少量甲基丙烯酸后,可使漆膜有更好的附着力,但过多容易发生交联。
三、主要仪器和药品
三口烧瓶(250ml)、球形冷凝管、滴液漏斗、温度计、量筒、玻璃棒、烧杯(200ml)。甲基丙烯酸甲酯、甲基丙烯酸丁酯、甲基丙烯酸、过氧化二苯甲酰、甲苯。
四、塑性丙烯酸酯的合成
(一)配方 : 质量份数g
甲基丙烯酸甲酯 30.0
甲基丙烯酸丁酯 68.0
甲基丙烯酸 2.0
过氧化二苯甲酰 0.5
甲苯 100
(二)操作步骤 :
1.蒸馏除去单体中的阻聚剂,然后将单体按配方混合。(暂时不做)
2.将100份甲苯加入反应瓶中,加热至90~95℃。
3.将过氧化苯甲酰溶于单体混合物中。
4.将单体混合物(已加引发剂)慢慢滴入热溶剂中进行聚合反应(滴加过程需要 1.5~2h),注意开始进行得慢一些。聚合反应开始后温度允许由于反应放热而稍有升高,但应注意控制滴加速度勿使升得太快,滴加完毕,温度一般在90~850℃之间。
5.在回流温度下保持2小时,控制不挥发份47 .5%以上,倒出物料。
五、注意事项:
l.开始滴加时应放慢速度,否则滴加了大部分单体后尚未开始聚合,待开始聚合时,因单体浓度过高,会突然剧烈反应放出大量热,出现危险。
2.滴加速度也影响分子量的大小和分子结构的均匀度,滴得慢时分子量较小但分子结构可能均匀,滴得快时分子量较大,分子结构均匀性较差。
3.配料及引发剂比例必须准确,对分子量影响很大。
4.引发剂用量及反应温度对反应时间有直接影响,引发剂用量高,温度高,只需较短时间就可得到较高转化率;引发剂用量少,反应温度低,必须延长保温时间以满足转化率要求,一般要求转化率不低于95%。反应过程中通过测定粘度确定反应进行情况。
5.清洗滴液漏斗,以免树脂聚合使仪器难以打开。
六、性能测试
测试粘度、固体物含量。
粘度:涂—4粘度计测试。
固体物含量:表面皿称量,120℃烘干1小时。
实验 4 聚醋酸乙烯酯乳液的合成
一、实验目的
1.了解自由基型加聚反应的原理。
2.掌握聚醋酸乙烯酯乳液的合成原理和方法。
二、实验原理
1.主要性质和用途
聚醋酸乙烯酯(polyviny acetate,简称PVA)乳液别名白乳胶,本品为乳白色粘稠浓厚液体,具有优良的粘接能力,可在5℃~40℃的温度范围内使用。具有良好的成膜性,且无毒、无臭、无腐蚀性,但耐水性差。
本品主要用于木材、纸张、纺织等材料的粘接以及掺入水泥中提高强度,也用作醋酸乙烯酯乳胶涂料的原料。
2.合成原理
醋酸乙烯很容易聚合,也很容易与其他单体共聚。可以用本体聚合、溶液聚合、悬浮聚合或乳液聚合等方法聚合成各种不同的聚合体,用于各个方面。醋酸乙烯酯单体的聚合反应是自由基型加聚反应属连锁聚合反应,整个过程包括链引发、链增长和链终止三个基元反应。链引发就是不断产生单体自由基的过程。常用的引发剂如过氧化合物和偶氮化合物,它们在一定温度下能分解生成初级自由基,它与单体加成产生单体自由基,其反应式为:
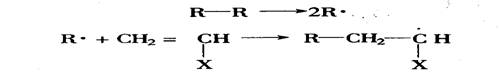
链增长反应就是极为活泼的单体自由基不断迅速地与单体分子加成,生成大分子自由基。链增长反应的活化能低,故速度极快。其反应式为
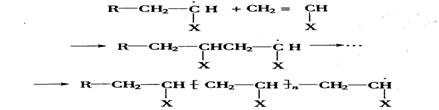
链终止反应是由两个自由基相遇,活泼的单电子相结合而使链终止。终止反应有两种方
式:
偶合终止:
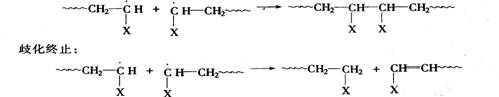
通常本体聚合、溶液聚合和悬浮聚合都用过氧化苯甲酰和偶氮二异丁腈为引发剂,而乳液聚合则都用水溶性的引发剂过硫酸盐和过氧化氢等。悬浮聚合和乳液聚会都是在水介质中聚合成醋酸乙烯的分散体,但两者之间有明显的区别。
悬浮聚合一般用来生产分子量较高的聚醋酸乙烯,用少量聚乙烯醇为分散剂,用过氧化苯甲酰等能溶解于单体的引发剂,聚合反应是在分散的单体的液滴中进行的,一般制得颗粒约在0.2mm-1.0mm的聚合物珠体,所以也有称之谓珠状聚合。
乳液聚合是在乳化剂的胶束中进行的,并不是在水相乳化的单体液滴进行的。而乳液聚合的产物(乳胶粒子)通常是在0.2μm~5μm粒度的乳胶液。
三、主要仪器和药品
三口烧瓶(250ml)、球形冷凝管、滴液漏斗、温度计、量筒、玻璃棒、烧杯(200ml)。
醋酸乙烯酯、聚乙烯醇17--99、乳化剂OP--10、K--12、邻苯二甲酸二丁酯、过硫酸钾、碳酸氢钠。
四、实验内容
1.聚醋酸乙烯乳液的配方
醋酸乙烯酯单体 46 邻苯二甲酸二丁酯 5
聚乙烯醇 2.5 蒸馏水 45.0
乳化剂OP—10 0.5 过硫酸钾 0.12
乳化剂K—12 0.25 碳酸氢钠 0.15
2.制备工艺
将聚乙烯醇与蒸馏水加入三口烧瓶中加热至80℃,搅拌使溶解完全。加乳化剂搅拌溶解均匀。之后加入醋酸乙烯单体总量的20%与过硫酸钾用量的40%,待温度至80℃~83℃且回流减少时,开始以每小时加入总量20%左右的速度连续加入醋酸乙烯单体。控制在1 h~2 h左右将单体加完。控制反应温度在78℃~82℃,每小时加入过硫酸钾用量的25%~30%。加完单体后加入余下的过硫酸钾,因放热体系温度升至 85℃,保温 30 min。冷至 50℃以下先后加入10%的碳酸氢钠水溶液和邻苯二甲酸二丁酯,控制 PH=6,搅拌30 min,冷却即为成品。
五、注意事项
1.过硫酸钾在每次加入时用水溶解成水溶液。
2.醋酸乙烯单体必须是新精馏过的,因醛类和酸类有显著的阻聚作用,聚合物的分子量不易增大,使聚合反应复杂化。
3.乳液聚合中都用水溶性引发剂,如过硫酸盐和过氧化氢,本实验用过硫酸钾。
4.聚乙烯醇是聚醋酸乙烯乳液聚合的最常用的乳化剂,能降低单体和水的表面张力,提高单体在水中的溶解度。
5.在按上述配方操作时,开始反应时加入过硫酸盐作引发剂,由于聚合反应过程中回流和连续缓慢加入单体,温度可在一段时间内无需加热或冷却即可保持在80℃左右。反应继续进行,需补加少量过硫酸钾以维持反应温度不下降。经过反复试验,就能在不同的设备条件下摸索出最适宜的加单体的速度、回流大小、每小时补加过硫酸钾的数量等操作控制条件,使反应温度稳定在78℃~82℃之间,使聚合反应能平稳地进行。所以在实际操作过程中需要很好地控制热量平衡。操作时如果反应剧烈,温度上升很快,则应少加或不加过硫酸钾,并适当加快单体加入速度。如温度偏低,则就要稍多加些过硫酸钾,并适当减慢单体的加入速度。反之就要适当减慢加入单体的速度,甚至暂时停止片刻,待回流正常后再继续加人单体。
单体加完后加入较大量的引发剂,使温度升至 85℃,并保温 30 min,目的是要尽可能地减少最后未反应的剩余单体量,这对乳液的稳定性和乳胶的质量是有利的。因为游离单体在存放中会水解而产生醋酸和乙醛,使乳液的pH值降低,影响乳液和乳胶的稳定性。一般在9 X 104 Pa真空下抽 lh~2 h能使残余单体减少至1%以下。
将乳化剂水溶液先和单体一起搅拌乳化,再加人引发剂引发聚合虽也可以,但在诱导期过后反应十分激烈,要做成质量好的乳液十分困难。因此可以先将乳化好的乳液放一部分在反应器内,加入部分引发剂引发聚合,然后慢慢连续加入乳化好的乳化液,并定时补加一定量的引发剂。
六、性能测试
测试粘度、PH值、固体物含量。
粘度:涂—4粘度计测试。
PH值:PH试纸测试。
固体物含量:表面皿称量,105℃烘干水分和残余单体。
七、思考题
1. 聚醋酸乙烯单体的聚合是什么反应?
2. 为什么聚醋酸乙烯聚合的单体必须新精馏?
3. 本实验的引发剂是什么?为什么要分期加入?
4. 聚乙烯醇在聚醋酸乙烯合成反应中有什么作用?
5.
实验 5 苯乙烯的自由基悬浮聚合
自由基聚合反应属连续聚合反应,活性中心是自由基。自由基聚合是合成高分子化学中极为重要的反应。其合成产物约占总聚合物的60%、热塑性树脂的80%以上,是许多大品种通用塑料、合成橡胶及某些纤维的合成方法。
一、目的要求:
本实验将通过对苯乙烯单体的自由基悬浮聚合,了解自由基聚合的不同实施方法,并对不同的方法和结果进行比较。
二、原理:
自由基聚合反应包括链引发、链增长和链终止三个部分,当体系中含链转移剂时,还可引起链转移反应,引起聚合物的分子量的降低。各部分简述如下:
(-)链引发:
链引发反应是形成单体自由基的反应,热、光、高能辐射等均可直接使单体产生自由基,但较常用的是从容易分解成自由基的化合物(引发剂)来得到。引发剂主要是过氧化物和偶氮化合物,在加热条件下分为两个自由基。
(1)引发剂I分解产生初级自由基:
I kd 2R·
(2)初级自由基与单体加成,生成单体自由基:
R·+M ------ki------RM·
因为ki>>kd,所以反应(1)决定了整个引发速率,表示为ki =2f kd,式中f为引发效率,表示引发剂分解产生初级自由基并与单体加成的部分。分解速率常数kd或半衰期t1/2表示引发剂的活性,kd越大或t1/2越小,则引发剂活性越高。在科研中,引发剂活性常用kd(秒-1)表示,但在工程技术上,则常以t1/2表示。
不同的引发体系应选用不同类型的引发剂。引发剂的分解反应为吸热反应,引发剂的选择与聚合温度密切相关,聚合温度高,可选用低活性引发剂,反之,则选用高活性引发剂,使自由基形成速率适中。
(二)链增长:
链引发形成的单体自由基,能继续与单体反应,生成大分子自由基。由于链增长反应活化能低,故链增长速率极快,约在0.01至几秒内,即可使聚合度达到103---04,所以聚合体系中存在的或是未反应单体,或是已生成的高分子,不存在聚合度递增的一系列中间产物。
RM·+M———RMM·———Mn·­­‑‑‑‑‑‑M(n+1) ·
假定不同链长的自由基活性相等,则链增长速率几为:
Rn= -d[M]/dt = kp[M][M·],式中[M]为单体浓度.[M·]为自由基浓度。当聚合体系中含有两种或多种单体时,则生成含有两种或多种单体单元的共聚物,形成共聚反应。共聚物的组成与体系中各单体的浓度、单体及其自由基的反应活性密切相关。
(三)链终止:
当两个自由基相遇,活泼的孤单电子相互作用可使链增长终止。其中又有双基偶合终止和歧化终止两种形式。
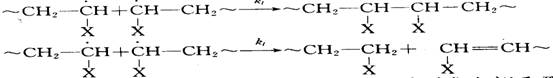
终止速率Rt=2kt[M·]2, 根据稳定态假设(Ri=Rt)(Ri为引发速率)和聚合物长链假定(Ri<<Rp=,可导出总聚合速率方程式:
Rp=kp[f kd/kt]1/2[I]1/2[M]
上式表明,聚合速率与引发剂浓度的平方成正比,与单体浓度的一次方程成正比。
此外,自由基聚合中还可发生链转移反应,即链自由基从单体、溶剂、引发剂甚至从大分子链上转移出一个原子,使链自由基本身终止,便使失去原子的分子成为新的自由基,并继续增长形成新的活性链。
链转移的结果,是聚合物的分子量降低,但自由基数目不变,若链转移所产生的自由基的活性和原自由基相同,则聚合中速率不变,利用此性质可控制产物的分子量。若前者的活性减弱或失活,则会出现缓聚或阻聚现象。为了防止单体在储存时发生聚合,常常在其中加入一定量的阻聚剂如硝基苯、苯醌等。在聚合反应前,上述阻聚剂必须彻底除去。
链式自由基聚合的实施方法主要有本体聚合、溶液聚合、悬浮聚合以及乳液聚合。本体聚合是单体本身加入(或不加)少量引发剂的聚合;溶液聚合是将单体和引发剂溶于适当溶剂中进行的聚合反应;悬浮聚合一般是将单体以液滴状悬浮于水中的聚合;乳液聚合则是单体在水中以乳液状态进行的聚合。以上几种不同的聚合方式比较如表1。
表l 不同聚合方式比较
内容 |
本体聚合 |
溶液聚合 |
悬浮聚合 |
乳液聚合 |
主要成分 |
单体,引发剂, |
单体,引发剂,溶剂 |
单体,引发剂,分散剂,水 |
单体,引发剂,乳化剂,水 |
引发剂 |
油溶性 |
油溶性 |
油溶性 |
水溶性 |
聚合场所 |
本体内 |
溶液内 |
单体液滴内 |
胶束和乳胶粒内 |
温度控制 |
难 |
较易,溶剂为带热体 |
易,水为带热体 |
易,水为带热体 |
聚合机理 |
遵循自由基聚合一般机理,分子量控制较因难,分子量分布较宽 |
可伴有向溶剂的链转移,速率较小.分子量较易控制,分子量分布较窄 |
与本体聚合相同 |
具有特殊机理,能同时提高聚合速率和聚合物分子量,分子量较易控制 |
产品特征 |
产物纯净,可直接成型,宜生产透明,浅色制品 |
聚合液一般直接利用 |
直接得到粒状产物,产物较纯净,可能留有少量分散剂,利于成型 |
产品含少量乳化剂及其他肋剂,用于典型要求不高的产品 |
主要工业生产品种 |
合成树脂: LDPE,HDPE,PS,PVC,PMMA,PP |
合成树脂: PAN,PVAC,HDPE, PP,合成橡胶 |
合成树脂: PVC,PS,PMMA |
合成树脂: PVC,PVAC,及其共聚物. PMMA及其共聚物. 合成橡胶 |
不同要求的产品,可通过不同的聚合方法来得到。有关本体聚合和溶液聚合,将分别在以后的实验中讨论,本实验将重点讨论悬浮聚合。
悬浮聚合实质上是借助于较强烈的搅拌和悬浮剂的作用,将单体分散在不溶的介质中,单体以小液滴的形式进行本体聚合;在每个小液满内,单体的聚合过程和机理与本体聚合相似。悬浮聚合解决了本体聚合中不易散热的问题,产物容易分离、清洗,可得到纯度较高的颗粒状聚合物。工业上用悬浮聚合生产的聚苯乙烯是一种易定型的热塑性高分子材料,其分子量分布较宽,制品有较高的透明性和良好的耐热性及电绝缘性。
三、仪器和试剂:
仪器:三口瓶,球形冷凝管,水浴锅,表面皿、吸管、移液管、搅拌器等。
试剂:苯乙烯、过氧化二苯甲酰(BPO)、聚乙烯醇(PVA)、去离子水、羧甲基纤维素钠CMC。
四、实验步骤:
1.悬浮聚合:
用分析天平准确称取 0.4gBPO放于100ml锥形瓶中,用移液管移取 16ml苯乙烯,加入到锥形瓶中,轻轻摇动,待BPO完全溶解于苯乙烯后将溶液倒入三口瓶。再加入25ml
2%的PVA溶液。最后用130ml去离子水分别冲洗锥形瓶和量简后加入三口瓶中。通冷凝水,启动搅拌器并控制转速恒定,在20~30min内将温度升至85℃,开始聚合反应。
在整个过程中,既要控制好反应温度,又要控制好搅拌速度。反应进行一个多小时后,体系中分散的颗粒由于聚合度的增加而变得发粘,这时搅拌速度忽快忽慢或停止都会导致颗粒粘在一起,或粘在搅拌器上形成结块,致使反应失败。
反应1.5~2小时后,如这时珠子已向下沉,可升温至85~90℃,用吸管吸取少量颗粒于表面皿中冷却观察,如颗粒已变硬发脆,表明大部分单体已聚会,可结束反应。
停止加热,撤出加热器,在搅拌状态下用冷水将反应体系冷却至室温。停止搅拌取下三口瓶。产品用布氏漏斗滤干,并用热水洗涤数次,冷水洗涤数次,洗去颗粒表面的分散剂。产品在50℃烘箱中烘干,称重并计算产率。
五、结果与讨论:
1.悬浮聚合的产物颗粒的大小与分散剂的用量及搅拌速度有关,严格控制搅拌速度和温度是实验成功的关键,为了防止产物结团,可加入极少量的乳化剂以稳定颗粒。若反应中苯乙烯的转化率不够高,则在干燥过程中颗粒中会出现小气泡,可利用在反应后期提高反应温度并适当延长反应时间来解决。
六、思考题:
1.结合悬浮聚合,说明配方中各组分的作用。
2.分散剂的作用原理是什么?改变用量会产生什么影响?
3.对比乳液和悬浮聚合的特点。
参考资料:
[1] EI麦卡弗里著,蒋硕健等译.高分子化学实验室制备.科学出版社,1981
[2] 复旦大学高分子科学系,高分子科学教研所编著.高分子科学技术(修订版).复旦大学出版社,1996
[3]胡学贵编著.高分子化学及工艺学.化学工业出版社,1991

